由香港科技大學晨興生命科學教授兼香港神經退行性疾病中心主任葉玉如教授領導的國際研究團隊,發現了一種在阿爾茲海默症(Alzheimer’s disease,簡稱AD)發病機制中起關鍵作用的血液蛋白,有助設計創新治療策略,降低AD發病風險和改善AD患者病況。
降低sST2含量 有助預防腦退化
目前,AD是一種不可逆轉的疾病,且沒有有效治療方法,正影響全球逾5000萬人口。其中一個關鍵障礙是,此病症的致病機制複雜且有許多未知之處,可用於開發藥物的有效靶點很少。早前有研究發現,AD患者大腦中的免疫細胞(小膠質細胞),無法有效清除有害的澱粉樣蛋白斑(Aβ),導致神經細胞功能失調,引起記憶喪失和認知障礙。至於排毒障礙的原因還有待深入探索。
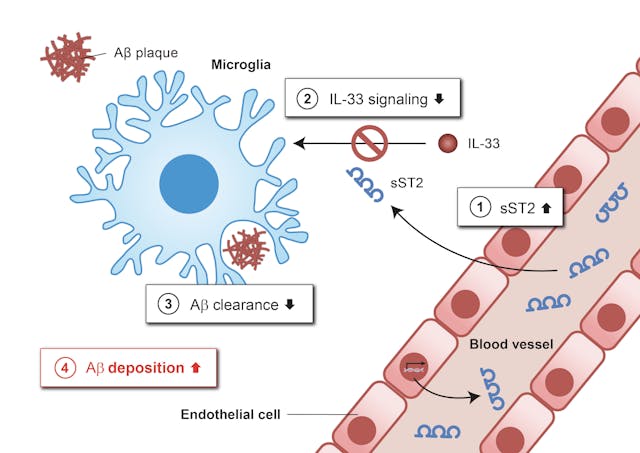
近日,葉教授領導的研究團隊發現,血液中的可溶性ST2(sST2)蛋白在抑制小膠質細胞的Aβ清除起着關鍵作用。隨着年齡增長,血液和大腦中sST2蛋白含量的增加會擾亂細胞因子白介素33(IL-33)的功效,降低小膠質細胞清除Aβ的能力,導致Aβ累積。研究團隊於較早前已經發現IL-33在大腦中能夠促進小膠質細胞對Aβ的清除,從而起到有益的功效。而是次團隊進一步發現,降低體內sST2含量則有助防護患上AD,以及改善AD相關病理。
sST2蛋白水平受遺傳影響
同時,研究團隊還發現,sST2蛋白水平受遺傳因素影響。其中,帶有rs1921622基因變異的人士即使在年齡增長時,其血液和大腦中的sST2蛋白含量依舊會處於相對較低水平,因而罹患AD的風險亦較低。這種情況在帶有APOE4基因突變的女性中尤為明顯(APOE4是AD的最強遺傳風險因素 )。根據團隊所做的腦部屍檢研究,帶有rs1921622基因變異的人士在罹患AD時病理特徵較為輕,即Aβ斑塊沉積較少,反映其大腦中的小膠質細胞可以更有效地清除Aβ。
綜合而言,這些重要發現揭示降低sST2蛋白水平可以是治療AD的一種方法,有助研發創新治療策略。該創新策略只須調控血液中的蛋白,與其他針對大腦的AD治療策略相比,更簡單更安全,亦為帶有APOE4基因突變的女性等高危人群帶來希望。據統計,帶有APOE4基因突變的女性,在AD患者中佔25%至50%,她們罹患AD風險更高,發病後症狀更嚴重。
葉玉如教授:為新藥開發提供靶點
葉教授說:「是次研究進一步提高了我們對AD發病機制的理解, 並為AD新藥開發提供了重要靶點。由此可見,精準醫學對於治療這種多因素導致的複雜疾病至關重要。下一步工作是開發針對sST2的臨床干預措施,評估其在預防和治療AD方面的可行性,特別是帶有APOE4基因突變、發病風險較高的女性。」
這項研究獲香港特區政府的InnoHK計劃支持,並由科大、倫敦大學學院和史丹福大學研究團隊,以及威爾士親王醫院、墨爾本大學和伊迪斯可文大學的臨床專家合作進行。研究成果近日刊載於國際權威科學期刊《自然-衰老》,並在Alz forum等關注AD 研究的學術交流平台引發熱議。






































