全球中藥市場達300億美元,但中國中藥的市場佔有率僅5%,中藥國際化幅度強差人意,故而與國藥素質參差有關,另一根本問題是欠缺一套國際公認的中藥標準,無法與國際市場接軌。臨危受命,港商被中央政府委以重任,與全球權威藥品標準機構美國藥典委員會(United States Pharmacopeia)共商中藥標準。為什麼是港商而非內地商人?香港在中藥國際化及標準化上扮演什麼角色,對本港中藥業及整體經濟發展,帶來哪些啟發?
中成藥國際化裹足不前
中藥國際化最先於1996年提出,2001年中國加入世界貿易組織後更見熱情,可是附加值較高而被視為國際化標誌的中成藥,七成出口傾斜於亞洲,按次為非洲及美洲,香港則居亞洲榜首。有別於低端產品,中成藥質量須達國際標準方可在其他國家或地區註冊及銷售,成功註冊象徵素質與國際水平看齊。可是,目前在歐盟成員國獲上市許可予以銷售的千多個植物藥品中,中國中成藥僅得兩個品種成功註冊;至於9家中藥企業經年在美進行註冊,迄今未見「零的突破」。
整體而言,國藥出口金額、數量、種類、地區,均顯示國際化幅度偏低。2017年中藥及中成藥出口金額僅82億人民幣,在內地中藥整體銷售額8000億中微不足道,2013至2017年間出口金額及數量分別跌一成及三成,見下圖。
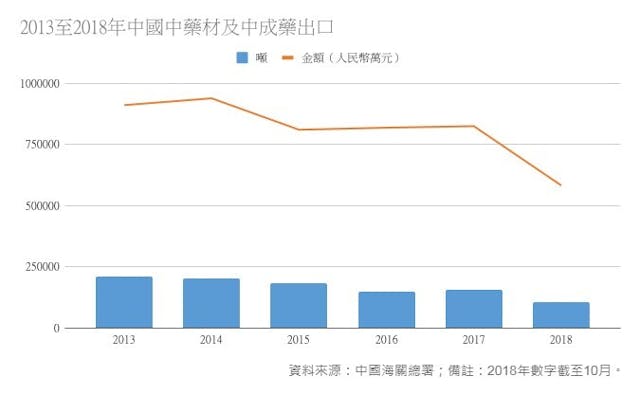
出口類別則以草藥及提取物等低端藥品為主,與中成藥的出口比例為三比一,處於供應鏈末端。國藥競爭力不足,那邊廂的日本及韓國生產的中藥品,卻壟斷了九成國際市場份額,日本更漸取代中國,成為美國最大進口來源地。
中央政府將開拓中藥國際市場列為中藥發展的戰略目標,可是出口業績不甚理想,其一故而是藥品質量欠佳,無法通過西方藥檢標準,而中藥材的重金屬及農藥殘留物同樣未符國際安全標準。中國商務部市場秩序司發表《2017中藥材流通市場分析報告》中透露,因品質問題被日本、韓國、美國、歐盟扣留和退回達44次之多,然而這相比2016年的56次,以及2015年的100多次已大幅減少。故此雖然中藥(中成藥及藥材)價錢廉宜,唯品質欠佳,影響人們對藥效及安全性的信心,也在國際市場形成對國藥的負面印象,難以獲消費者垂青。其二是未有一致的中藥標準,這不獨是品質是否達標的問題,更涉及複雜的中西醫藥體系,難免與話語權扯上邊。究竟香港從中可扮演什麼角色?
中藥標準話語權 港商有話兒
歐盟成員國中僅法國及徳國承認植物藥,鐘擺另一端的西班牙對之完全不予認可,採中間路線的荷蘭和比利時以及正準備脫歐的英國,則與美國制度相近,允許植物藥以膳食補充劑及保健品等名義進入市場。無疑門檻相較成藥為低,產品無需與西藥標準看齊;有辣有不辣,既為保健品自然不得作功能性及治療性的聲稱,公眾無從得知產品安全性。這正是念慈庵枇杷膏的遭遇,儘管品質優良在華人社會流傳百年,卻因未清晰交代藥效,在美國被西醫質疑會食死人。因此中成藥能夠堂堂正正以藥的名義進入國際市場,仍然是業界甚或中國政府的最終目標。
但並不代表標準化等於西藥化,硬套西藥標準制定中藥標準。得需承認中藥材在不同氣候及環境下種植,質量本身存有差異。而有別於單方西藥由單一分子組合,中藥採複方,由數種中藥配成藥劑,可產生不同組合,在烹煮過程中又會釋放不同物質,產生質變。再者,現時檢測標準採西方分析化學的標準,與中藥按臨床療效總結結論,十分不同。有兩點值得關注:首先由原料以至生產及效能測試等各個環節,中西藥體系大相徑庭;其次是中藥十分複雜,難以訂立一套檢定質量,安全和藥效的客觀標準。中西藥原理迥異,將西藥原理套在中藥,令後者表現出處處不達標,形象負面,窒礙中藥國際化。
雖則2013年成都地奧制藥的心血膠囊在荷蘭成功註冊,實現了歐盟傳統藥註冊「零的突破」,大部份仍未能以藥的形式進入歐美市場,天津天使力製藥的丹參滴丸早於90年代已在美國申請註冊,20年過去仍處於臨床試驗階段,經年痴痴等待,成功與否仍為未知數。這帶出了一個重要問題,中藥標準如何與國際社會的藥物註冊標準接軌,進行國際化。藥品質量達標是底線,無退讓餘地,透過科學化實驗對成份進行標準化,訂立一套科學化指標用以鑑定中藥有效性和安全性,加強中藥規範性,為建立中藥標準話語權創造條件。只有品質被認可,才有堅持中藥體系及理論別於西藥的獨特性的話語權,將中藥打造為中國的文化品牌,形成國際話語權,讓質優的中藥品及中華文化走向世界。
日本與聯合國教科文組織共同於1994年提出《奈良真實性文件》的個案很值得參考,如何以不亢不卑態度指出東西方文化及社會發展相異,在文物價值釐定上存有不同價值觀,若僅以1964年制定的《維尼斯憲章》(Charter of Venice)作準,往往形成不協調,建議在釐定價值時建基多個元素。一,文化多樣性是人類共同的精神及智慧成果;二,尊重不同文化及社會價值,在釐定文物價值時將之置於其所屬文化體系內;三,多方合作就價值達致共識,而非一言堂。文件並不是要挑戰公約,乃是將其精神延伸,回應現代社會的特有關注,這與中藥作為另類療法在全球興起,中國與國際市場需共同釐定中藥標準,既要回應消費者對藥品安全的關注,又要將標準置於中藥體系及中華文化傳統內考量,更要與國際標準接軌,乃同出一輒。當中吸收了國際市場對藥品的安全要求,亦堅持對文化多樣性的尊重,擴大以西藥為主流醫藥系統至包括中藥體系,增強中藥話語權。
與美國藥典委員會共商中藥標準,顯然成為爭取話語權的途徑之一。委員會就全球所生產、經銷、使用的藥品等,設立品質、純度、鑒定和濃度標準,並將之納入《美國藥典》。藥典被認為是高水準的質量標準,不但在美國獲認可,亦成為140多個國家公認的標準。有鑑藥典的權威性,獲其確認標準有助加快被國際社會認可,在中藥國際化滯後下,港資培力控股受中央政府委托,成為唯一代表與委員會商討中成藥質量和安全標準的釐定。

特殊地位與制度成香港突圍關鍵
為什麼是港商?客觀上,特區政府繼2002年起按世界衛生組織的標準實行藥材標準檢測,確保中藥品沒有農藥殘留及重金屬超標,將藥品質量提升至國際優質藥品製造標準,又於2010年確立標記藥材,「港標」不獨是品質的Q嘜認證,更是質量與國際水平看齊的象徵,品牌優勢賦與港商晉身為中國代表的條件。
由人文視野及國際網絡視之,雖然中國大門趟開多時,相比港商與國際市場進行貿易及接觸的歷史仍有距離,這點讓具國際視野的港商大有優勢。當然,個別企業的努力不容小覻,培力控股一直致力制定客觀的中藥複方審核及註冊標準,且常與海外國家藥檢當局溝通和商討。這三個層面均建基於香港品牌優勢,讓它在中藥國際化上及中國對外貿易上扮演不可或缺的角色。
原刊於《信報》,本社獲作者授權轉載。
發展中醫藥為支柱產業系列 5








































